Wie viele Menschen sterben in Deutschland an multiresistenten Erregern?
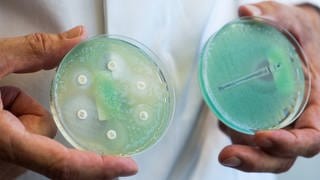
Laut einer Studie von 2018 gibt es in Deutschland jährlich etwa 2.400 Todesfälle durch resistente Erreger, viele davon im Krankenhaus. Je häufiger Antibiotika eingesetzt werden, desto mehr steigt die Wahrscheinlichkeit, dass sich eine Resistenz entwickelt. Und im Krankenhaus, vor allem auf der Intensivstation, werden und müssen viele Antibiotika eingesetzt werden.

Antibiotikaresistenzen sind ein weltweites Problem. In Subsahara-Afrika etwa ist das Problem insgesamt am größten. Entwickeln sich dort multiresistente Bakterien, dann können die auch hier zum Problem werden. Deswegen ist ein globaler Blick beim Kampf gegen Antibiotikaresistenzen nötig.
Warum werden keine neuen Antibiotika entwickelt, gegen die Bakterien nicht resistent sind?
Es werden regelmäßig neue Antibiotika entwickelt, die sind aber oft Varianten von welchen, die es bereits gibt. Die funktionieren zwar oft gut, aber Bakterien, die gegen das ursprüngliche Antibiotikum resistent sind, können dann relativ schnell neue Resistenzen entwickeln.
Eigentlich braucht es ganz neue Wirkstoffklassen. Davon gibt es aber so gut wie keine. Einerseits ist es einfach schwer neue Wirkstoffe zu finden – aber auch ein ganz wichtiger Grund ist: Es lohnt sich einfach nicht. Denn: Ein neues Antibiotikum, gegen das noch kein Bakterium resistent ist, würden nur im Notfall eingesetzt werden. Damit würde die Gefahr gesenkt, dass sich wieder neue Resistenzen entwickeln.
Das Medikament würde sich also nur kaum verkaufen und der Hersteller auf den Entwicklungskosten sitzen bleiben. Diese liegen in der Regel zwischen mehreren hundert Millionen und einigen Milliarden Euro. Sobald der Patentschutz auf das neue Antibiotikum abläuft, wird der Markt dann von Generikaherstellern geschwemmt. Diese müssen keine Entwicklungskosten wieder einbringen und können das Medikament dann viel günstiger anbieten. Das drückt den Preis auch für den Entwickler.
Ein Vorschlag, um das attraktiver zu machen, ist dass Unternehmen, die ein solches Antibiotikum entwickeln – dass die dann den Patentschutz für ein anderes ihrer Medikamente verlängern dürfen. Damit könnten sie dann nämlich die Entwicklungskosten wieder reinholen, auch wenn das Antibiotikum nicht eingesetzt wird.
Wie können Antibiotikaresistenzen verhindert werden?
Einerseits müssen weniger Antibiotika eingesetzt werden. Immer noch werden zum Beispiel bei einer Erkältung oft Antibiotika auf Verdacht verschrieben, falls es eine bakterielle Infektion ist, obwohl es wahrscheinlich eine Virusinfektion ist. Und da bringen Antibiotika überhaupt nichts.
Hausärzt:innen haben aber oft nur wenige Minuten Zeit für eine Entscheidung. Ein Bluttest im Labor untersuchen zu lassen, dafür ist keine Zeit. Um sich abzusichern verschreiben sie deshalb oft Antibiotika. Eine Lösung dafür wäre die Entwicklung sogenannter Point-of-Care-Tests – Testgeräte, die einfach zu bedienen sind und mit denen innerhalb von Minuten ermittelt werden kann, ob es sich um eine Virus- oder eine Bakterieninfektion handelt.

Andererseits dürfen Antibiotikabehandlungen aber auch nicht abgebrochen werden, etwa weil man sich wieder gesund fühlt und auf die weitere Einnahme verzichten will. Auch das gibt den Bakterien die Möglichkeit, Resistenzen zu entwickeln.
Wenn nach der Behandlung doch Tabletten übrig bleiben, dann dürfen diese nicht die Toilette runtergespült werden. Denn so kommen sie in die Umwelt, wo auch wieder Resistenzen entstehen können. Oft können Medikamente über den Restmüll entsorgt werden, manchmal kann man sie auch in der Apotheke oder dem Wertstoffhof abgeben. Informationen dazu gibt es in der Apotheke.
Gibt es Alternativen zu Antibiotika?
Es gibt einige spannende Ansätze, zum Beispiel Antikörpermedikamente. Außerdem arbeiten viele Hersteller gerade an sogenannten Immunmodulatoren, die sollen kurz gesagt das Immunsystem fit machen und hochfahren, dass es dann selbst mit den Keimen umgehen kann.
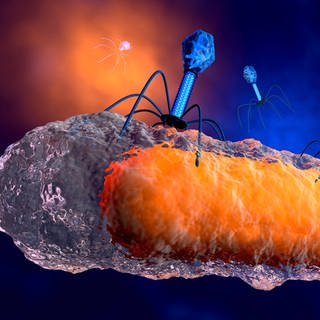
Interessant sind auch sogenannte Phagen bzw. Bakteriophagen. Das sind Viren, die Bakterien angreifen. Sie sind sehr speziell und können uns Menschen nicht infizieren. Ein Phagenmedikament hätte kaum oder sogar keine Nebenwirkungen.
Bis jetzt konnte allerdings noch gar nicht nachgewiesen werden, dass Phagen als Medikament überhaupt funktionieren. Ein solches Medikament wäre wahrscheinlich sehr individuell, also und müsste unter Umständen für jeden Patienten einzeln angepasst werden. Das würde diese Methode natürlich sehr teuer machen. Am besten würden sich die Phagen wahrscheinlich deshalb für chronische Erkrankungen eignen.
Die beste Alternative, die es zumindest für einige Bakterieninfektionen bereits gibt, ist eine Impfung. Wer gar nicht erst krank wird, braucht auch keine Medikamente.