Das Mainzer Biotechunternehmen Biontech hat gemeinsam mit dem Konzern Pfizer positive Wirksamkeitsdaten für seinen Corona-Impfstoff vorgelegt. Danach sinkt das Risiko nach der Impfung an Covid-19 zu erkranken um mehr als 90 Prozent im Vergleich zu Ungeimpften.
Vorläufig gutes Testergebnis für Corona-Impfstoff
Insgesamt erhielten in der laufenden internationalen Phase III Studie rund 22.000 Probanden den neuen RNA-Impfstoff, die anderen 22.000 erhielten eine Placebo-Spritze.
Bisher wurden in dieser Studie nur 94 Infektionsfälle beobachtet. Virologen halten das für ein sehr positives Ergebnis, das vermutlich zu einer baldigen Zulassung führen wird. Sie sprechen von großartigen, vielversprechenden Daten.
Bisher stehen allerdings noch keine Primärdaten zur Verfügung und eine Peer-Review-Publikation steht noch aus. Deshalb müssen zunächst weitere Details geprüft werden:
"Zum Beispiel bezüglich verschiedener Altersgruppen und in welchen Gruppen die 94 Fälle genau aufgetreten sind."
Nach einer Pressemitteilung der Unternehmen wurde der Impfschutz bereits 28 Tage nach Beginn der Impfung, die aus einem 2-Dosis-Schema besteht, aufgebaut. Eine wissenschaftliche Publikation ist offenbar in Vorbereitung.
Biontech und Pfizer sind damit die weltweit ersten Unternehmen, die erfolgreiche Daten aus der für eine Zulassung entscheidenden Studie mit einem Corona-Impfstoff vorgelegt haben.
Noch in diesem Monat wollen Biontech und Pfizer in den USA eine Notfallgenehmigung für den Impfstoff beantragen. Das ist möglich, wenn genügend Daten zur Sicherheit des Impfstoffs vorliegen. Das Unternehmen rechnet damit in der dritten Novemberwoche. Bislang seien in der Studie keine ernsten Sicherheitsbedenken aufgekommen.
EMA entscheidet über Notfallzulassung
Das Unternehmen Biontech steht bereits mit der Europäischen Arzneimittelagentur (EMA) in einem sogenannten rollierenden Verfahren. Das bedeutet, immer wenn durch die Impfstofftests neue Daten verfügbar sind, erhält sie sofort die Behörde, so dass sie in Echtzeit überprüft werden können. Die EMA kann dann basierend auf diesen Ergebnissen über eine Notfallzulassung entscheiden.
Paul-Ehrlich-Institut ist am Datencheck beteiligt
Ein Impfstoff erhält nur dann eine Zulassung, wenn nachgewiesen ist, dass er wirksam und verträglich ist. Für Europa wird das zentralisierte Zulassungsverfahren für Covid-19-Impfstoffe durch die Europäische Arzneimittelagentur EMA koordiniert. Die Impfstoffbewertung der EMA nehmen die Expertinnen und Experten der nationalen Arzneimittelbehörden Europas vor, also auch die Experten des deutschen Paul-Ehrlich-Instituts. Dabei werden Qualität, Wirksamkeit und Sicherheit der Impfstoffe gründlich untersucht und bewertet.

BioNTech hat bereits Impfstoff vorproduziert
Biontech-Chef Ugur Sahin hat bereits am 30. Oktober der dpa erklärt, Biontech habe schon angefangen, Impfstoff zu produzieren. Dieser Impfstoff werde im Unternehmen gelagert. Wenn eine Impfstoff-Zulassung vorliege, dann könne die Freigabe dieser Impfstoffdosen schrittweise erfolgen. Theroretisch könne das auch noch im Jahr 2020 stattfinden.
Der neue Impfstoff heißt BNT 162b2
Für die Entwicklung des Impfstoffes mit dem Kürzel BNT 162b2 haben Biontech und Pfizer bis zu 375 Millionen Euro Sonderförderung von der Bundesregierung erhalten. Mit den Produktionsanlagen von Pfizer könnten bis Ende 2021 rund 1,5 Milliarden Dosen des Impfstoffes hergestellt werden, heißt es aus dem Unternehmen. Mehrere hundert Millionen Dosen sind schon vorab verkauft worden - in die USA, nach Japan und nach Kanada.

Das neue Impfstoff-Verfahren von Biontech
Das Team von Biontech und Pfizer hat einen neuartigen genbasierten Impfstoff gegen das Corona-Virus entwickelt. Klassische Impfstoffe enthalten meist abgeschwächte Viren oder Teilstücke davon. Sie rufen dann im Körper die gewünschte Abwehrreaktion gegen den Erreger hervor. Bei den neuen genbasierten Impfstoffen ist das anders: hier steckt gar kein Virusmaterial im Impfstoff.
Statt Virusmaterial wird ein Botenstoff für Erbinformation geimpft
Stattdessen liefert die Spritze nur den Bauplan für ein bestimmtes, ungefährliches Virusprotein. Das funktioniert mit Hilfe sogenannter messenger RNA, kurz mRNA – also über einen Botenstoff für Erbinformation. Biontech und andere Hersteller zielen dabei auf das sogenannte Spike-Protein. Das ist die stachelige Hülle des Coronavirus. Dieses Protein stellt der Körper nach der Impfung dann eigenständig her. Das Immunsystem bildet daraufhin Abwehrstoffe gegen den Eindringling und soll danach vor Sars-Cov2 geschützt sein.
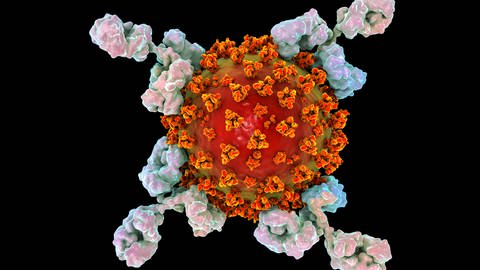
Impfstoff dieser Art ist eine Weltneuheit
Bisher ist allerdings weltweit noch kein einziger Impfstoff dieser Art zugelassen. Der neue, genbasierte Ansatz gilt als besonders elegant: Denn jeder Geimpfte produziert das entscheidende Wirk-Element selbst, im eigenen Körper. Deshalb können Pharmafirmen wie Biontech, Curevac und Moderna ihre mRNA-Impfstoffe auch schneller herstellen als die Konkurrenz, die auf klassische Impfverfahren setzt.
Neuer Impfstoff braucht extrem kalte Lagertemperatur
Allerdings haben Impfstoffe mit Boten-RNA auch einen Nachteil: Sie müssen extrem kalt gelagert werden. Biontech zum Beispiel geht von Minus 80 Grad aus. Bei normaler Kühlschranktemperatur hält der Impfstoff bisher nur ein paar Tage. Eine erste Genehmigung des Impfstoffes hält Biontech-Chef Sahin Ende dieses oder Anfang nächsten Jahres für möglich. 50 Millionen Impfdosen können es dieses Jahr werden, für nächstes Jahr sind 1,3 Milliarden Dosen geplant.
Verteilung des Impfstoffes könnte Monate oder Jahre dauern
Biontech will eine „faire Verteilung“, das heißt es soll nicht danach gehen, welches Land zuerst Impfstoff bestellt hat. Dann würden nämlich die USA schneller beliefert als Deutschland. So soll es nicht laufen. Aber wer wann wieviel Impfstoff bekommt, ist noch unklar. Weil der Impfstoff bei minus 70 Grad gelagert werden muss und voraussichtlich erstmal nur in 60 großen Impfzentren gespritzt wird, wird es schätzungsweise eher Frühjahr oder Sommer 2021 werden, bis die ersten geimpft sind. Ganz Deutschland zu impfen dauert Monate, manche schätzen sogar ein bis zwei Jahre.

